В Корее смогли редактировать нейронные цепи мозга с помощью астроцитов, открыв путь к лечению аутизма и шизофрении
- 6 дней назад
- 6 мин. чтения
Корреспондент Гу Бон Хёк
- Институт фундаментальных наук (IBS) и Институт исследования мозга Южной Кореи разработали технологию «SynTrogo» для целенаправленной «обрезки» синапсов


Схема технологии «Синтрого», позволяющей реконструировать нейронные цепи путем точного удаления определенных синапсов [Предоставлено IBS]
Разработана революционная технология, позволяющая улучшить память путем редактирования «нейронных цепей» в мозге. Ожидается, что ее использование в будущем откроет новый этап в лечении дегенеративных заболеваний мозга, таких как аутизм и шизофрения.
Совместная исследовательская группа из Института фундаментальных наук (IBS) и Корейского института исследования мозга (KBRI) разработала технологию «SynTrogo», позволяющую с помощью астроцитов точно удалять определенные синапсы и реконструировать нейронные цепи в мозге.
Мозг человека состоит из «коннектомов», в которых триллионы синапсов образуют комплексную цепь, соединяясь с друг другом. Это служит основой для когнитивных процессов, таких как память, эмоции и суждения. До сих пор исследования мозга сосредоточивались на регулировании передачи информации между нейронами через синапсы, а редактирование самого коннектома — канала, по которому протекает информация — считалось невозможным.
Исследователи, вдохновившись явлением «трогоцитоза» (Trogocytosis), при котором иммунные клетки отрывают и удаляют лишь часть соседней клетки, словно пожирая ее, создали синтетический белок, искусственно вызывающий этот процесс.
Они разработали систему, в которой в синапсах нейронов экспрессируется зеленый флуоресцентный белок (Green Fluorescent Protein, GFP), а в астроцитах — рецептор GFP-наноантител, связывающийся с ним, чтобы обеспечить прочное соединение между двумя типами клеток. В результате астроцитам удалось эффективно захватывать и удалять целевые участки синапсов.
Когда исследовательская группа применила технологию Syntrogo к нейронным цепям гиппокампа мышей, плотность синапсов снизилась примерно на 27 %. Сначала может показаться, что уменьшение количества синапсов приводит к снижению функций мозга, однако «количественное уменьшение» привело к «качественному улучшению»: размеры сохранившихся синапсов увеличились, а их функции значительно усилились.
В частности, значительно возросла доля шипиков (Spine), оснащенных шипиковым аппаратом (Spine Apparatus), который играет ключевую роль в нейропластичности, благодаря чему нейронные цепи были реорганизованы таким образом, чтобы более надежно передавать сигналы.
Кроме того, было зафиксировано усиление долговременной потенциации (long-term potentiation), которое характеризуется укреплением нейронных связей, что свидетельствует об улучшении нейропластичности и способности к обучению всей нейронной цепи.

Рис. 2: SynTrogo, индуцированный модифицированными взаимодействиями между нейронами и астроцитами.
a Флуоресцентные изображения SynTrogo (SynT) культивируемых нейронов, вызванного астроцитами посредством взаимодействий лиганд-рецептор. Масштабные линейки: 50 мкм (слева), 10 мкм (справа). b Количественная оценка поглощения GFP астроцитами во время SynT. n = 18 астроцитов в группе. c Изображения в режиме замедленной съемки поглощения фрагмента нейрональной мембраны, меченной лигандом, астроцитом, экспрессирующим рецептор. Масштабная линейка, 5 мкм. d Флуоресцентные изображения и 3D-реконструкции, демонстрирующие поглощение эндогенных синаптических молекул (слева, Bassoon; справа, Homer1) астроцитарным SynT. Масштабная линейка, 20 мкм (большие изображения), 5 мкм (малые изображения). e Количественная оценка сигналов Bassoon и Homer1 в астроцитах, экспрессирующих рецептор. n = 10 (Ctrl), 24 (SynT) клеток для Bassoon; 5 (Ctrl), 15 (SynT) клеток для Homer1. Изображения в режиме замедленной съемки культивируемых нейронов, коэкспрессирующих лиганд либо с f Synaptophysin (SYP)-TagBFP, либо с g TagBFP, вместе с астроцитами, экспрессирующими рецептор, в условиях SynTrogo. Масштабные линейки: 20 мкм (слева), 5 мкм (справа, увеличенные изображения) и 2 мкм (внизу, увеличенные изображения). Желтые стрелки на левых изображениях указывают на области интереса (ROI), в которых видны поглощенные GFP-положительные везикулы с сигналами TagBFP или без них. Время указано в часах:минутах. Данные представлены в виде медианы с межквартильным размахом; пунктирные линии в (b, e). Статистическая значимость определялась с помощью непарного t-критерия для (b) и множественного непарного t-критерия для (e).

Рис. 3: SynTrogo пресинаптических аксонов CA3, осуществляемый астроцитами CA1.
a Схема действия SynTrogo (SynT), нацеленного на аксоны CA3 и астроциты CA1. В область CA3 вводили аденоассоциированный вирус (AAV), экспрессирующий лиганд под контролем промотора CaMKIIα. В CA1 вводили AAV, экспрессирующие мембранозависимый RFP (Lck-RFP) или рецептор под промотором GfaABC1D. Мозг анализировали с помощью иммуногистохимии через 3 недели после инъекции. b Флуоресцентные изображения сигналов лиганда и рецептора в CA1. Масштабные линейки: 50 мкм. c Сигналы лиганда с GFAP и либо мембранным маркером (контроль), либо рецептором (SynT). Масштабные линейки, 20 мкм. d Интенсивность GFP внутри и снаружи территорий астроцитов. N = 3 мыши в группе; n = 12 (внутри), 7 (снаружи) областей интереса (ROI) (Ctrl); 7 (внутри), 7 (снаружи) ROI (SynT). e 3D-визуализация астроцитов в Ctrl или SynT. Масштабная линейка, 5 мкм. f Объемное соотношение (v/v) лиганда GFP к соме астроцита (S100β). N = 3 мыши в группе; n = 42 (Ctrl), 64 (SynT) астроцита. g Флуоресцентные и 3D-изображения, показывающие лиганд GFP и VGluT1 в пределах территорий астроцитов. Масштабная линейка, 5 мкм (большой); 2 мкм (увеличенные изображения). h Нормализованная интенсивность синаптических маркеров в пределах территорий сомы астроцитов. N = 4 мыши в группе; VGluT1: n = 30 (Ctrl), 33 (SynT); PSD95: n = 31 (Ctrl), 29 (SynT) клеток; VGAT: n = 33 (Ctrl), 35 (SynT) клеток; Гефирин: n = 40 (Ctrl), 33 (SynT) клеток. i Корреляция между уровнями лиганда GFP и пресинаптических маркеров в пределах территорий астроцитов (n = 36 клеток). j Флуоресцентные изображения синаптического маркера. Масштабные линейки, 10 мкм. Количество синапсов VGluT+ и VGAT+ в пределах k территорий астроцитов и l слоя CA1 SR. N = 3 мыши в группе. Для k: VGluT1, n = 39 (Ctrl), 43 (SynT); VGAT: n = 26 (Ctrl), 40 (SynT) астроцитов. Для l, VGluT1: n = 103 (Ctrl), 99 (SynT); VGAT: n = 99 (Ctrl), 98 (SynT) областей визуализации. Данные представлены в виде медианы с межквартильным размахом в (d, f, h, k, l). Статистическая значимость определялась с помощью двустороннего ANOVA с тестом Фишера LSD для множественных сравнений для (d); непарного t-теста (f, k, l); множественных непарных t-тестов для (h); и простой линейной регрессии с F-тестом для (i).
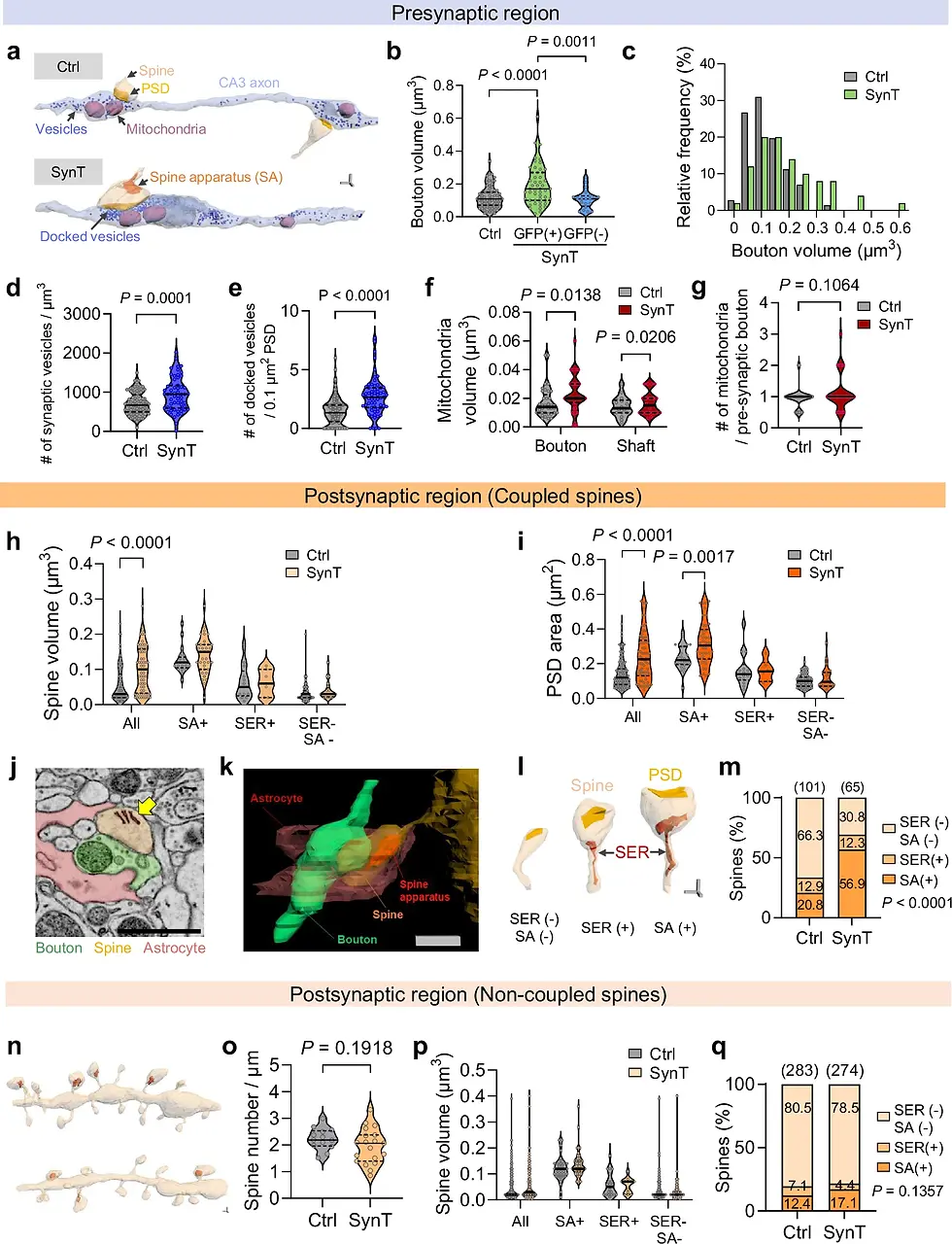
Рис. 7: Структурная перестройка пре- и постсинаптических компартментов после синаптической редукции, связанной с SynTrogo.
a 3D-рендеры электронно-микроскопических изображений синаптического содержимого. Масштабная линейка — 0,2 мкм. Объем бутона (b), распределение объемов (c), общее количество синаптических везикул (d) и пристыкованных везикул (e) в пресинаптических бутонах. N = 3 мыши в группе; b, c: n = 71 бутон в группе Ctrl, 50 в группе GFP+ SynT, 20 в группе GFP– SynT; d: n = 85 бутонов в группе Ctrl, 59 в группе SynT; e: n = 94 бутона в группе Ctrl, 61 в группе SynT. f Объем митохондрий в аксональных бутонах или стволах. g Количество митохондрий в пресинаптических бутонах (N = 3 мыши в группе; Ctrl: n = 37 бутонов, 16 стволов; SynT: n = 39 бутонов, 22 ствола митохондрий). Объем шипиков (h) и площадь PSD (i) в дендритных шипиках, соединенных с лиганд-мечеными аксонами (N = 3 мыши в группе). Для h: Ctrl, n = 25 SA(+), 14 SER(+), 78 SER(−) SA(−); n = 42 SA(+), 8 SER(+), 21 SER(−) SA(−) шипиков. Для i: Ctrl, n = 25 SA(+), 14 SER(+), 70 SER(−) SA(−); SynT, n = 42 SA(+), 6 SER(+), 22 SER(−) SA(−) шипиков. j Электронно-микроскопическое изображение шипикового аппарата (стрелка). Масштабная линейка, 1 мкм. 3D-реконструкции отростка астроцита, бутона и шипика (k), а также типичные SER(−) SA(−), SER(+) и SA(+) шипики (l). Масштабная линейка, 0,5 мкм (k), 0,2 мкм (l). m Процентное распределение шипиков SER(−) SA(−), SER(+) и SA(+) (n = 101 Ctrl, 65 SynT шипиков). n–q Анализ несвязанных дендритов. n 3D-изображения дендритов и шипиков. Масштабная линейка, 0,2 мкм. o Плотность шипиков несвязанных дендритов (n = 13 Ctrl, 19 дендритов SynT). p Объем шипиков (Ctrl: n = 35 SA(+), 20 SER(+), 228 SER(−) SA(−); SynT: n = 47 SA(+), 12 SER(+), 215 SER(−) SA(−) шипиков). q Процентное распределение подтипов шипиков (хи-квадрат). Данные представлены в виде медианы с межквартильным размахом в (b, d–i, o, p). Статистическая значимость определялась с помощью одностороннего ANOVA с тестом множественных сравнений Тьюки для (b); непарного t-теста для (d, e, g, o); двустороннего ANOVA с тестом множественных сравнений Сидака для (f, h, i, p); и критерия хи-квадрат для (m, q).

Совместная исследовательская группа, проводившая данное исследование. Ли Сан Гю (слева направо), младший главный исследователь Департамента по исследованию памяти и глиальных клеток IBS; Ли Чан Чжун, руководитель Департамента по исследованию памяти и глиальных клеток IBS; доктор Ли Ге Чжу из Корейского института исследования мозга. [Предоставлено IBS]
Результаты экспериментов на животных, проведенных исследователями, тоже показали, что у мышей, на которых была применена технология Syntrogo, воспоминания о страхе, сформированные слабым раздражителем, сохранялись более ярко и дольше, а после стирания памяти они демонстрировали способность гибко заменять старые воспоминания новыми, не зацикливаясь на прежних.
«Мы выяснили фундаментальный принцип, по которому мозговые цепи самостоятельно адаптируются и усиливают свои функции даже в условиях уменьшения количества синапсов» - сказал Ли Ге Чжу, ведущий научный сотрудник Корейского института исследования мозга, добавив: «Это даст важные подсказки для восстановления когнитивных функций в различных моделях заболеваний мозга».
«Данное исследование станет новой платформой для лечения шизофрении или аутизма, возникающих из-за аномалий в количестве синапсов, а также дегенеративных заболеваний мозга, характеризующихся потерей синапсов» - отметил руководитель департамента Ли Чан Чжун.
Результаты исследования опубликованы 15 апреля в международном научном журнале «Nature Communications».




Комментарии