Корейские ученые смогли из черного паслена получить диосгенин – сырье для стероидных гормонов – с выходом на уровне диоскорея
- 24 февр.
- 7 мин. чтения
Корреспондент Гу Бон Хёк
- KAIST и Национальный университет Кёнсан смогли перепроектировать метаболические пути посредством генетической модификации черной паслен

Профессор Ким Сан Гю (слева направо) и доктор Им Сан Бу, которые провели данное исследование [Предоставлено KAIST]
Паслен черный - сорняк, часто встречающийся на обочинах дорог и пустырях - стал ценным сырьем для гормональных препаратов, необходимых в современной медицине.
Корейский институт передовых технологий (KAIST) сообщил, что исследовательская группа во главе с профессором Ким Сан Гю из факультета биологических наук в ходе совместных исследований с командой профессора Пак Сун Чжу из Национального университета Кёнсан смогла регулировать гены крестовника для эффективного производства «диосгенина» - сырья для кортикостероидов (противовоспалительных и иммуномодулирующих препаратов) и половых гормонов (контрацептивов и гормональных препаратов).
Диосгенин является основным исходным материалом в современной фармакологии. Он используется в качестве синтетического сырья для стероидных гормональных препаратов, широко применяемых в повседневной жизни, таких как противовоспалительные средства и средства от зуда. В настоящее время он в основном извлекается из корней «диоскореи», но данное растение требует нескольких лет для сбора урожая и трудно поддается генетической манипуляции, что ограничивает расширение масштабов производства.
Чтобы преодолеть эти ограничения, исследовательская группа сосредоточила свое внимание на «черном паслене», который имеет короткую продолжительность поколения (около трех месяцев) и легко поддается генетической модификации. Черный паслен естественным образом производит «соласодин», токсичное стероидное соединение. Исследователи отметили, что данное вещество по своей структуре очень похоже на диосгенин.
Команда использовала технологию редактирования генов CRISPR-Cas9 для корректировки определенного гена паслена черного, «SnGAME4». Это заблокировало метаболический путь, ведущий к токсичному соединению, перенаправив метаболический поток в производство диосгенина. Кроме того, они подавили другой ген черного паслена «SnGAME25», который регулирует реакцию в тканях листьев, тем самым максимально увеличив накопление диосгенина как в плодах, так и в листьях.

Паслен черный, используемый в качестве лекарственного сырья. Изображение сгенерировано искусственным интеллектом [Предоставлено KAIST]
Примечательно, что в этом исследовании был использован процесс «естественного брожения». В нем используется собственный фермент растения, бета-глюкозидаза (SaF26G), который преобразовывает компонентов в легкоизвлекаемую форму. В результате команда смогла повысить уровень диосгенина в зеленых плодах растения до значения, сопоставимого с диоскореей, которая на данный момент служит промышленным сырьем.
Благодаря применению «технологии повышения урожайности плодов (мутация гена S)», разработанной исследовательской группой Национального университета Кёнсан, урожайность плодов на одно растение значительно увеличилась. Это также создало промышленную основу, позволяющую производить большее количество фармацевтического сырья на одной и той же площади.

Мутация SnGAME4 и связанные с ней метаболические изменения. (a) Паттерн мутации SnGAME4 в отдельных мутантных линиях Sngame4-1 и Sngame4-2. Сайты-мишени gRNA показаны красным цветом, а изменения последовательности выделены синим цветом. (b, c) Метаболические профили гликозидов соласодина и производных диосгенина в зеленых плодах WT (черный) и мутанта Sngame4 (красный). Хроматограммы экстрагированных ионов представлены с использованием основных ионов соласодина (m/z 414,5 > 396,5) и диосгенина (m/z 415,3 > 271,25). Оси Y указывают относительную интенсивность. Основные пики пронумерованы, а молекулярные структуры проиллюстрированы. Протодиосгенин представляет собой производное диосгенина фуростанольного типа. Масс-спектры (d) (2) α-соламаргина и (e) (5) протодиосцина из экстрактов общего сапонина. Ось x указывает значения m/z, а ось y — относительную интенсивность, нормализованную к самому высокому пику. Основные фрагменты обозначены синим цветом, а различия в массе между фрагментами отмечены стрелками. Предполагаемые места расщепления показаны на основе масс-спектров. Gal, D-галактоза; Glc, D-глюкоза; Rha, L-рамноза.

Структурная идентификация и преобразование с помощью β-глюкозидазы посредством самопроизвольного брожения. (а) Общие экстракты сапонина из зеленых плодов Sngame4, измеренные с помощью MRM диосгенина до и после самопроизвольного брожения. Хроматограммы экстрагированных ионов представляют основной ион диосгенина (m/z 415,3 > 271,25). Ось y указывает относительную интенсивность, нормализованную к самому высокому пику каждого образца. Основные пики в каждом образце пронумерованы. (b, c) Химические структуры и схемы фрагментации (b) фунлиозида B и (c) триллина. Места расщепления обозначены пунктирными стрелками. (d) Диагностические ионы для фунлиозида B (m/z 577,30 > 415,25, фиолетовый) и триллина (m/z 577,40 > 433,25, зеленый) в экстрактах общего сапонина до и после самопроизвольного брожения. Пропорция шкалы оси y между каждым диагностическим ионом одинакова для всех образцов. (e) Превращение протодиоцина в диоцин под действием β-глюкозидазы и самопроизвольное закрытие F-кольца. (f, g) Относительная концентрация (f) протодиоцина и (g) диоцина в отсутствие спонтанной ферментации (No SF), при спонтанной ферментации (SF) и при спонтанной ферментации с добавлением 100 мМ глюконо-δ-лактона (SF+GDL). Площадь каждого пика MRM протодиоцина и диоцина была нормирована по сухой массе образца. Данные представляют среднюю концентрацию (± SD) с тремя биологическими повторениями. Статистическая значимость была определена с помощью одностороннего ANOVA, за которым последовал тест множественного сравнения Тьюки. (h) Выход диосгенина оценивался с помощью кислотного гидролиза с или без обработки спонтанной ферментацией. Данные представляют среднюю концентрацию (± SD) с четырьмя биологическими повторениями. Статистическая значимость была определена с помощью двустороннего непарного t-теста (***, p < 0,001). ESI, электрораспылительная ионизация; GDL, глюконо-δ-лактон.

Идентификация и функциональная характеристика SaF26Gs. (a) Уровни экспрессии ортологов StF26G в S. americanum, расположенных на хромосоме 6, показаны в виде log10(TPM+1). Каждая колонка представляет отдельные биологические репликаты от трех разных растений. (b, c) Экстрагированные ионные хроматограммы (b) протодиоцина (m/z 1031,4 > 253,3) и диоцина (m/z 869,4 > 147,0), и (c) фунлиозида B (m/z 577,3 > 415,25) и диосгенина (m/z 415,3 > 271,25). Пунктирные линии обозначают стандарты, а сплошные линии представляют реакции с каждым лизатом (EV, лизаты из листьев, проникнутых пустым вектором; SaF26G.L1, лизаты из листьев, экспрессирующих SaF26G.L1). Ось y обозначает относительную интенсивность по отношению к самым высоким пикам, а пропорции шкалы оси y для каждой ионной пары одинаковы для всех образцов. (d) Изменения уровня экспрессии SaF26Gs в растениях, подвергшихся вирус-индуцированному генному заглушению (VIGS), рассчитанные по значениям Ct RT-qPCR (eGFP, растения, инфильтрированные TRV2-eGFP; SaF26G, растения, инфильтрированные TRV2-SaF26G). Данные представляют среднюю концентрацию (± SD) из трех биологических повторений. Статистическая значимость определялась с помощью двустороннего непарного t-критерия (***, p < 0,001). (e–g) Анализ лизатов в сочетании с VIGS. (e) Уровни оставшегося протодиоцина при инкубации протодиоцина с лизатами. (f) Уровни произведенного диоцина при инкубации протодиоцина с лизатами. (g) Уровни оставшегося диоскина при инкубации диоскина с лизатами. Данные представляют среднюю концентрацию (± SD) из трех биологических повторных опытов. Статистическая значимость была определена с помощью одностороннего ANOVA с последующим тестом множественного сравнения Туки. DC, диоскин; MRM, мониторинг множественных реакций; PDC, протодиоскин; STD, стандарт.

Подавление SnGAME25 перенаправляет метаболизм листьев в сторону гликозидов протодиосгенина. (a) Уровни экспрессии ортологов SlGAME25 в S. nigrum, представленные в виде log10(TPM+1). Каждая колонка представляет отдельные биологические репликаты от трех отдельных растений. (b) Изменения в уровнях экспрессии SnGAME25 были рассчитаны на основе значений RT-qPCR Ct. Данные представляют среднюю концентрацию (± SD) из трех биологических повторений. Статистическая значимость была определена с помощью двустороннего непарного t-критерия (**p < 0,01). (c, d) Экстрагированные ионные хроматограммы (c) тигогенина (m/z 417,30 > 273,25) и (d) диосгенина (m/z 415,30 > 271,25) MRM из образцов, обработанных VIGS. Ось y представляет собой относительную интенсивность по отношению к самым высоким пикам. Основные пики обозначены цифрами. (e, f) Масс-спектры (e) соединения (7) и (f) соединения (8). Ось y — относительная интенсивность по отношению к наиболее распространенному фрагменту. Основные ионы-фрагменты обозначены синим цветом, а различия в массе между ключевыми фрагментами обозначены стрелками. Различия между основными ионами указаны над каждой стрелкой. Предполагаемые места расщепления показаны на основе масс-спектров. MRM, мониторинг множественных реакций.
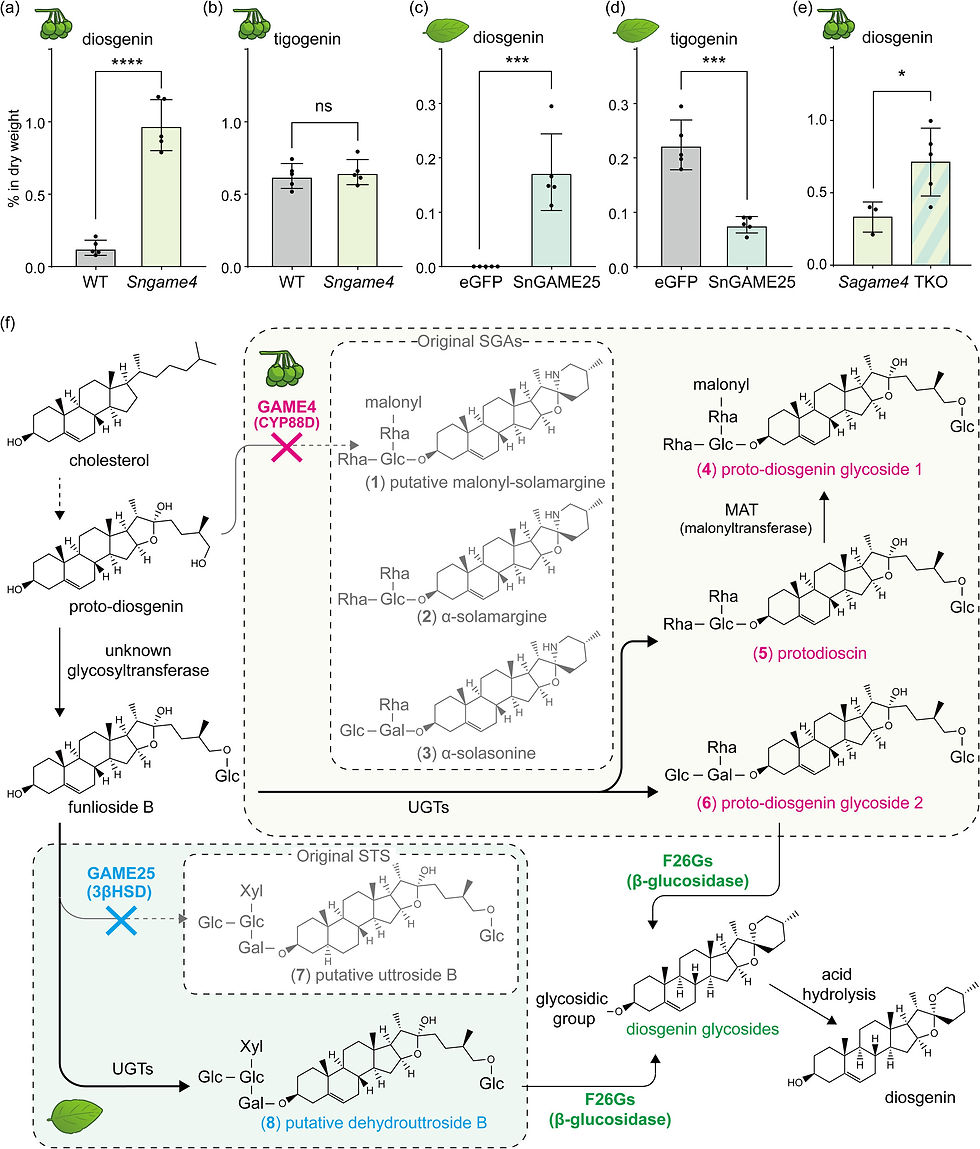
Улучшение выхода агликона и обзор метаболических изменений. (a–e) Конечный выход диосгенина и тигогенина, выраженный в процентах от сухого веса. (a) Выход диосгенина и (b) тигогенина в зеленых плодах S. nigrum, а также (c) выход диосгенина и (d) тигогенина в листьях, обработанных VIGS (растения, инфильтрированные eGFP, TRV2-eGFP; растения, инфильтрированные SnGAME25, TRV2-SnGAME25). (e) Выход диосгенина из зеленых плодов S. americanum Sagame4 и TKO (тройной нокаут-мутант SaGAME4, SaGAME25-1 и SaGAME25-2). Данные представляют собой среднюю концентрацию (± SD) из пяти биологических повторений, за исключением зеленых плодов Sagame4, биологических повторений которых три. Статистическая значимость определялась с помощью двустороннего непарного t-критерия. (*, p < 0,05; ***, p < 0,001; ****, p < 0,0001; ns, не значимо). (f) Схематическое представление перестройки метаболического пути, приводящей к усилению биосинтеза диосгенина в S. nigrum.

Перенаправление метаболического потока в S. lycopersicum. (a) Паттерн мутации SlGAME4 в двух независимых линиях мутантов S. lycopersicum. (b) Метаболический сдвиг в листьях от WT к мутанту Slgame4. Экстрагированные ионные хроматограммы представляют основные ионы продуктов методов MRM томатидина или тигогенина. Шкалы оси y согласованы в пределах каждого MRM. (c, d) Количественное определение (c) α-томатина и (d) производного неотигогенина в WT и мутантах Slgame4. Данные представляют среднюю концентрацию (± SD) из пяти биологических повторений. Статистическая значимость была определена с помощью одностороннего ANOVA с последующим тестом множественного сравнения Тьюки. (e) Изменение уровня экспрессии SlGAME25 в листьях S. lycopersicum, обработанных VIGS, измеренное с помощью RT-qPCR (eGFP, растения, инфильтрированные TRV2-eGFP; SlGAME25, растения, инфильтрированные TRV2-SlGAME25). (f) Уровень гликозида прото-ямогенина в листьях S. lycopersicum, обработанных VIGS. Статистическая значимость определялась с помощью двустороннего непарного t-критерия. (g, h) Общее количество сапонинов из листьев с подавленным экспрессией GAME25 (g) S. nigrum WT и (h) мутанта Slgame4 было экстрагировано до и после спонтанной ферментации и проанализировано с помощью LC–MS с использованием методов funlioside B и trillin MRM. Диагностические ионы обозначены цветом, а ось y представляет собой относительную интенсивность по отношению к самому высокому пику. Пропорции шкалы оси y между двумя диагностическими ионами одинаковы для всех образцов. Данные представляют среднюю концентрацию (± SD) из пяти биологических реплик, проникнутых TRV2-eGFP, и шести биологических реплик, проникнутых TRV2-SlGAME25. (i) Лизаты листьев WT S. lycopersicum и S. nigrum, содержащие равное количество общего белка, были подвергнуты реакции с протодиосцином, и концентрации протодиосцина и диосцина измерялись в несколько моментов времени. Данные представляют среднюю концентрацию (± SD) из трех биологических реплик. Статистическая значимость была определена для каждого временного интервала по сравнению с контролем с использованием множественного непарного t-критерия (*, p < 0,05; , p < 0,01; *, p < 0,001; ****, p < 0,0001).

Введение мутации GAME4 в мутантную линию S. nigrum с повышенной урожайностью. (a) Схема мутации SnGAME4s в мутантной линии s1/+s2s3+Sngame4. Места нацеливания gRNA показаны красным цветом, а изменения последовательности выделены синим цветом. (b) Морфология соцветий мутантных линий S. nigrum с повышенной урожайностью. Красные стрелки указывают на точки ветвления в соцветии. Масштабная линейка = 2 см. (c) Плодоносность линий мутантов Sngame4 и s1/+s2s3+Sngame4. Данные представляют среднюю концентрацию (± SD) из 12 биологических повторений. (d) Метаболический сдвиг зеленых плодов от s1/+s2s3 к s1/+s2s3+Sngame4. Показаны хроматограммы экстрагированных ионов основных продуктов соласодина (m/z 414,50 > 396,50) и диосгенина (m/z 415,30 > 271,25). Ось y представляет относительную интенсивность, нормализованную к самым высоким пикам. (e) Выход диосгенина из мутантов Sngame4 и s1/+s2s3 + Sngame4 после кислотного гидролиза. Данные представляют среднюю концентрацию (± SD) из пяти биологических повторений Sngame4 и шести биологических повторений s1/+s2s3 + Sngame4. Статистическая значимость определялась с помощью двустороннего непарного t-критерия (****, p < 0,0001; ns, не значимо).
«Данное исследование показывает, что путем тщательной переработки уникальных метаболических путей, присущих сорнякам, мы можем производить высокоценные лекарственные компоненты» - сказал профессор Ким Сан Гю, добавив: «Это поможет нам обеспечить сырье для фармацевтических стероидов более стабильным и экологически чистым способом».
Результаты исследования опубликованы 16 января в международном журнале по растениеводству «Journal of Plant Biotechnology».




Комментарии